Publié le 15 aoû 2016Lecture 9 min
Adénomyose et infertilité
M. ZITOUN(3), R. CABRY(1), F. SCHEFFLER(1), N. BELHADRI-MANSOURI(1), N. CELTON(1), M. BENKHALIFA(1), H. COPIN(1), J. GONDRY(2) – 1. Service de médecine et biologie de la reproducion – cytogénétique – CECOS de Picardie - 2. Service de gynécologie-obstétri
L’adénomyose est la présence anormale d’îlots endométriaux, entourés d’une prolifération de fibres musculaires lisses, au sein du myomètre au-delà de 2,5 mm par rapport à la cavité utérine. Le diagnostic de l’adénomyose repose désormais sur l’échographie et surtout l’imagerie par résonance magnétique (IRM). La confirmation de cette pathologie est histologique et elle se présente sous forme diffuse ou localisée (adénomyose focale ou adénomyome).
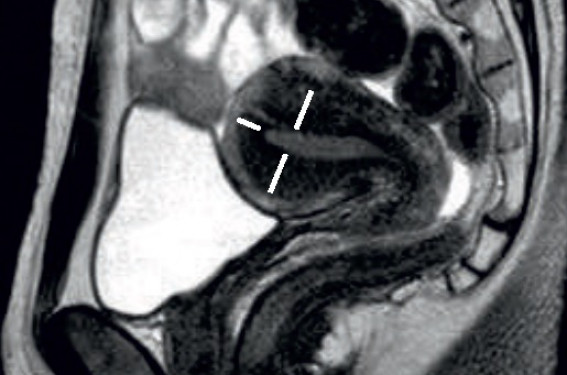
L'adénomyose touche les femmes de plus de 35 ans, avec une fréquence de 51 % entre 40 et 50 ans. Cependant, quelques cas d’adénomyose floride ou d’adénomyome ont été rapportés chez des femmes de moins de 20 ans(1). Les facteurs de risque de l’adénomyose sont la multiparité, les antécédents de curetage, de résection hystéroscopique et d’hystérotomie, une puberté après l’âge de 15 ans et une absence de contraception. Le recul de l’âge de la première grossesse (30 ans), le désir d’un deuxième enfant ou une nouvelle union, et son association à certaines pathologies pouvant également interférer avec la fertilité (myomes, hyperplasies de l’endomètre, endométriose externe) ont comme conséquence sa découverte de plus en plus fréquente dans un contexte d’infertilité et sa probable participation à celle-ci. Relations physiopathologiques de l’adénomyose avec l’infertilité L’adénomyose peut s’expliquer soit par une invagination de la partie profonde de l’endomètre à travers les fibres myométriales ou le long des lymphatiques intramyométriaux, soit par une métaplasie produisant de novo du tissu endométrial au sein du myomètre(2). Par ailleurs, des facteurs génétiques existent probablement pour prédisposer à la survenue de l’endométriose et de l’adénomyose. Il existe dans l’adénomyose une hyperestrogénie (en relation avec une hyperactivité de l’aromatase cytochrome P450), qui contribue au niveau de l’utérus à un hyperpéristaltisme et une hyperpression endocavitaire. Il s’ensuit des microtraumatismes disloquant l’endomètre basal et conduisant à son invagination dans l’archimyomètre, couche interne circulaire du myomètre, encore appelée zone de jonction (JZ ou ZP pour les Anglo-Saxons). La figure 1 rappelle que la patho-genèse de l’adénomyose et de l’endométriose externe est commune, en liaison avec cette dislocation de l’endomètre. Dans l’adénomyose, la ZP est le siège d’une réaction inflammatoire chronique médiée par les cytokines, les prostaglandines, l’ocytocine et des facteurs de croissance. Elle est aussi le lieu de contractions utérines interférant avec la différenciation endométriale, le transport spermatique et l’implantation(3). Kunz(4) a montré que la prévalence de l’adénomyose est de 79 % chez les femmes avec endométriose, passant à 90 % chez celles qui ont un conjoint fertile (défini comme ayant une mobilité de type « a » > 20 %), soit une différence significative (p < 0,01). Cet impact de l’adénomyose sur la fertilité peut s’expliquer par une perturbation du transport utérin des spermatozoïdes du fait des modifications de l’archimyomètre. Du fait de ces anomalies, l’adénomyose se caractérise par une perturbation de l’implantation embryonnaire. De plus, on note dans cette pathologie un taux élevé de radicaux libres dans la cavité utérine, un développement anormal de l’endomètre perturbant le métabolisme stéroïdien local et une perte des marqueurs de l’implantation : le LIF, la glycodéline, l’intégrine β3, l’ostéopontine et la vitronectine sont abaissés, tandis que l’IL-6, l’IL-10, l’IL-18 et le TNFα sont augmentés. Il a été montré également que, dans l’adénomyose, l’expression du gène HOXA 10 (essentiel pour la survie embryonnaire) est diminuée durant la phase sécrétoire, ce qui pourrait expliquer le faible taux de grossesses des femmes adénomyosiques(5). Enfin, dans l’adénomyose, à côté des perturbations endométriales, existe une modification de la vascularisation au niveau de l’endomètre eutopique et ectopique, avec une augmentation du VEGF et du HIF-1α (hypoxie inductible facteur 1α)(6). Figure 1. Physiopathologie de l’endométriose externe et de l’adénomyose, passant par le mécanisme commun de la dislocation de l’endomètre. A : androgènes ; E2 : estradiol ; OT : ocytocine ; P450 : aromatase cytochrome P450. Traitements pour améliorer la fertilité en cas d’adénomyose L’assistance médicale à la procréation (AMP) Cette pathologie est fréquente chez les femmes de plus de 38-40 ans prises en charge en AMP. Elle peut s’accompagner d’une perturbation de la fonction ovarienne avec augmentation des ovocytes immatures et d’un défaut d’implantation de l’embryon. Néanmoins, il semble que l’adénomyose ait un impact plutôt sur l’implantation embryonnaire (OR : 0,79 [0,67-0,93](7)) que sur la fécondation (OR : 1,01 [0,93- 1,10]), contrairement à l’endométriose externe. Maubon(8) a étudié 148 femmes ayant eu 253 transferts (232 en FIV et 21 TEC). Une IRM pelvienne avec une coupe sagittale permettait de définir 3 mesures de la ZP, antérieure, postérieure et fundique (figure 2). Figure 2. Adénomyose : imagerie par résonance magnétique (IRM) du pelvis, en coupe sagittale et séquence T2 : mise en évidence de la zone jonctionnelle (JZ ou ZP pour les Anglo-Saxons). Les tirets blancs indiquent les mesures antérieure, postérieure et fundique de la zone de jonction. Maubon (2010) : AJZ : moyenne des trois mesures ; MJZ : valeur maximale des trois mesures L’AJZ était la moyenne des trois mesures et la MJZ la valeur maximale des trois mesures. Après réalisation d’une courbe ROC donnant comme seuil de la MJZ la valeur de 10 mm, les taux de grossesses par transfert sont de 45 % pour une MJZ ≤ 10 mm (65 % des cas), de 16 % pour une MJZ entre 10 et 12 mm (25 %) et de 5 % si la MJZ est supérieure à 12 mm (10 %). L’odds ratio du taux de grossesses par transfert (MJZ ± 10 mm) est égal à 9 (3,2-29), indépendamment de l’âge, du nombre d’embryons transférés et de la qualité de ceux-ci. Les mêmes résultats sont observés avec une AJZ de ± 7 mm. En combinant ces deux paramètres (MJZ > 10 mm et AJZ > 7 mm), le taux de grossesses s’effondre à 2,4 % (contre 44,6 % avec les autres combinaisons), ce qui donne un OR : 32 (4,2-241) (p < 0,0001). Cet auteur propose donc la réalisation d’une IRM à la recherche d’une adénomyose après deux échecs de transfert, et incite à traiter par agoniste de la GnRH pendant 6 mois avant le transfert, ce qui contribue à diminuer la ZP, l’activité de l’aromatase cytochrome P450, l’infiltrat macrophagique et les radicaux libres. De même, Soares(9) a montré un effet délétère de l’endométriose et de l’adénomyose sur les chances de grossesse en cycle naturel, alors qu’il ne retrouve aucun impact lorsqu’une préparation endométriale a eu lieu par agoniste de la GnRH + estrogènes puis progestérone. Les études de Ferrero(10) et de Daraï(11) confirment l’effet délétère de l’adénomyose sur les chances de grossesse en FIV, même après résection d’un nodule rectovaginal (p < 0,04). À l’opposé, deux études retrouvent des résultats similaires avec ou sans adénomyose. Dans celle de Mijatovic(12), 74 patientes infertiles ont été traitées chirurgicalement pour endométriose et prises en charge en FIV, ICSI avec un protocole ultra-long (3 mois) d’agoniste de la GnRH. Seules 20 femmes présentaient une adénomyose, ce qui est faible. De plus, il n’existait pas de groupe contrôle où les femmes avec adénomyose n’étaient pas traitées par des agonistes de la GnRH avant FIV/ICSI. Costello(13) a rapporté une étude en FIV/ICSI avec protocole agoniste long entre 37 femmes avec adénomyose diagnostiquée à l’échographie et 164 sans adénomyose. Il ne retrouvait aucune différence en ce qui concerne la réponse ovarienne à la stimulation (10 ovocytes récupérés), les taux de grossesses évolutives (29,7 vs 29,3 %) et les taux de fausse couches spontanées (15,4 vs 27,1 %), mais ici encore, l’effectif des femmes avec adénomyose est faible et les deux groupes déséquilibrés. Dans ce même contexte, se situe l’étude de Salim(14) qui retrouve des résultats totalement opposés dans son étude prospective sur l’impact de l’adénomyose diagnostiquée par l’échographie en FIV/ICSI. Deux cent cinquante-six femmes constituaient le groupe témoin et 19 étaient atteintes d’adénomyose. Les taux de grossesses cliniques et évolutives sont significativement (p < 0,001) inférieurs en cas d’adénomyose, respectivement 22,2 vs 47,2 % et 11,1 vs 45,9 %. Le taux de fausse-couches spontanées (FCS) est significativement plus élevé dans le groupe adénomyose (50 vs 2,8 % ; p < 0,001). D’autres études sont rapportées dans le tableau ci-dessous. Traitement chirurgical Le traitement chirurgical de l’adénomyome est plus indiqué que les traitements chirurgicaux conservateurs des adénomyoses extensives, efficace sur les douleurs mais avec un très faible taux de grossesses. Des études ont montré les effets positifs des agonistes de la GnRH ± chirurgie (adénomyomectomie : 50 % de grossesses(15)). Al-Jama(16) a comparé deux groupes, l’un traité par agoniste par chirurgie (exérèse microchirurgicale des adénomyomes), puis agoniste 6 mois. Après un suivi de 3 ans, les taux de grossesses étaient respectivement de 13,6 % dans le premier groupe et 44,4 % dans le 2e groupe (p = 0,0393). Cette différence en termes de taux de grossesses pourrait s’expliquer par la récidive des adénomyomes et de l’adénomyose à l’arrêt des agonistes, comme cela est observé en cas de traitement préopératoire pour des myomes. En conclusion L’adénomyose est responsable de perturbations physiopathologiques qui diminuent les chances de grossesse, mais son effet au cours de la prise en charge en FIV/ICSI est atténué par la prescription de protocoles longs ou ultra-longs avec les agonistes de la GnRH. Certains auteurs signalent une augmentation des FCS, peut-être en rapport avec l’activité myométriale particulière de cette pathologie. Dans les prochaines années, les SPRM (selective progesterone receptor modulators), molécules agonistes/antagonistes du récepteur de la progestérone pourraient apporter un bénéfice, car ils entraînent une amélioration des douleurs et une régression des lésions dans l’endométriose, sans entraîner d’hypo-estrogénie(17).
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :