Sénologie
Publié le 07 sep 2011Lecture 11 min
Apport de l’IRM mammaire dans le dépistage des cancers du sein
B. SALICRU, Clinique du Mail, Grenoble
Parallèlement à la mise en place en France d’un dépistage de masse, avec un cahier des charges rigoureux prévoyant la réalisation d’une mammographie tous les 2 ans à partir de 50 ans, il apparaissait manifeste que ce type de surveillance était insuffisant pour répondre à un risque de cancer du sein survenant plus tôt dans la vie et selon une fréquence accrue pour certaines populations. Il était logique d’envisager une prise en charge plus adaptée de ces patientes. L’IRM mammaire, examen particulièrement sensible et non irradiant, déjà utilisée avec succès dans un certain nombre d’indications, est alors apparue comme une arme supplémentaire dans la détection des lésions mammaires dans cette population jeune, particulièrement exposée.
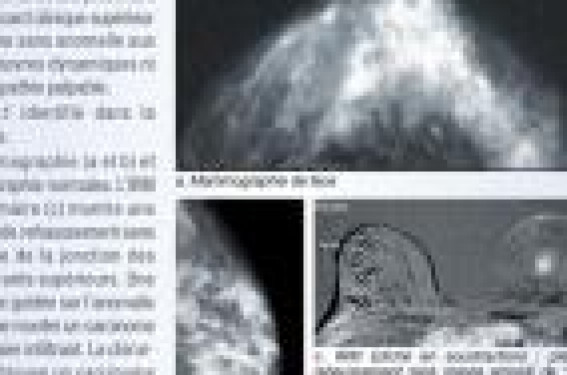
Actuellement, le risque de cancer du sein cumulé sur la vie est de 10 % pour l’ensemble de la population générale féminine. De longue date, des facteurs de risque ont été identifiés pour le cancer du sein chez la femme et leurs contributions relatives établies de manière plus ou moins précise selon les études (1). Ainsi, dans la population générale, le facteur de risque le plus important reste l’âge, puis l’histoire familiale, hormis dans le cas d’une prédisposition héréditaire avérée chez une femme porteuse d’une mutation identifiée dans un des gènes majeurs de susceptibilité tel que BRCA1 et BRCA2, avec un risque relatif supérieur. Performances de l’IRM Les performances de l’IRM ont été colligées récemmen t(2) dans le Rapport d’évaluation technologique (mars 2010) édité par la Haute Autorité de Santé (HAS). Les éléments de synthèse cidessous sont extraits de cette somme bibliographique et résument les performances de l’IRM, bien établies par la littérature internationale. Détection des lésions (cas clinique n°1) Les valeurs de sensibilité, spécificité, valeurs prédictives positive et négative de l’IRM mammaire sont plus grandes que celles de la mammographie (et/ou de l’échographie) dans l’évaluation de la présence de lésions cancéreuses (8 études) : – la sensibilité de l’IRM varie de 86 à 100 % ; – la sensibilité de la mammographie varie entre 56 et 86 % ; – la sensibilité de l’échographie varie entre 75 et 97 %. Cela est vrai pour les cancers invasifs (18 études) et pour les cancers in situ (CCIS) (3 études) et ce, quelle que soit la taille de la tumeur (2 études). Ces résultats ne remettent pas en cause les performances actuelles du dépistage de masse des cancers du sein, qui est adapté à une population plus âgée, mais permettent de comprendre l’intérêt d’utiliser l’IRM pour explorer des seins spontanément plus délicats à explorer par mammographie. L’absence d’irradiation est également un élément qui a compté. Évaluation de la taille tumorale La taille tumorale estimée à l’IRM, comparativement à la taille tumorale estimée à la mammographie, est mieux corrélée à la taille réelle retrouvée à partir de la pièce histologique (10 études). La fréquence de sous-estimation de la taille des lésions est moindre avec l’IRM ; toutefois, elle surestime la taille tumorale comparativement à la mammographie (1 étude). Évaluation de la multifocalité ou de la multicentricité La détection de la multifocalité et de la multicentricité est meilleure avec l’IRM qu’avec les techniques d’imagerie conventionnelle (5 études). L’IRM détecte des lésions supplémentaires (non vues à la mammographie ou à l’échographie) chez environ 1 patiente sur 5. La sensibilité de l’IRM est de 100 % dans toutes les études (4 études et une métaanalyse regroupant 19 études). Évaluation de la bilatéralité Dans l’évaluation de la bilatéralité, l’IRM a une bonne sensibilité et spécificité (8 études et une métaanalyse de 18 études), mais 2 études et une métaanalyse rapportent une valeur prédictive positive (VPP) < 50 % pour l’IRM, nécessitant le recours à la macrobiopsie guidée sous IRM. Celle-ci doit faire partie de l’arsenal diagnostique au même titre que les autres techniques de prélèvement sous peine de perdre tout intérêt aux performances diagnostiques de l’IRM. Une métaanalyse rapporte une fréquence de détection de lésions supplémentaires dans le sein controlatéral de 4 %. Notion de score de risque du cancer du sein dans la population Mutations BRCA1 et BRCA2 et autres Ces mutations concernent 1 femme sur 1 000 (population ashkénaze : 1/50). Leur transmission est de type autosomique dominant. Les risques de cancer du sein et de l’ovaire, à l’âge de 70 ans, sont respectivement pour BRCA1 de l’ordre de 65 et 40 % et, en cas de mutation du gène BRCA2, de l’ordre de 45 et 10 %. D’autres mutations plus rares sont connues, mais seuls des tests génétiques destinés à l’identification de mutations des gènes BRCA1 et BRCA2 sont proposés aux patientes avec une histoire personnelle et/ou familiale évocatrice d’une prédisposition génétique majeure : précocité de l’âge au diagnostic, atteintes bilatérales et/ou multifocales, antécédents familiaux multiples de cancer du sein, notamment associés à ceux de l’ovaire. Ces deux gènes sont impliqués pour une proportion marginale des cancers du sein, probablement moins de 5 %, mais trouvent toute leur importance dans le fait que les sujets à risque sont particulièrement jeunes et de ce fait ne bénéficieraient pas d’une surveillance adaptée sans la connaissance du risque génétique. Risque familial Dans 60 à 80 % des cas de cancers familiaux, aucune mutation de gènes n’est mise en évidence. C’est l’intérêt de la consultation génétique d’estimer, grâce à divers scores (score de Gail-NCI, modèle de Claus (1994), modèle BRCAPRO (1995-98) : basé sur BRCA, modèle IBIS, etc.), le risque tumoral pour une situation familiale donnée. En pratique quotidienne, le clinicien utilisera le score INSERM pour diriger une patiente vers la consultation génétique (tableau 1). Au-delà d’un score INSERM de 5, une patiente pourra bénéficier d’une consultation génétique. Efficacité du dépistage par IRM Les performances de l’IRM étant bien établies, encore fallait-il envisager la place de l’IRM mammaire dans le dépistage des cancers du sein. Introduire cette technique dans le dépistage de masse ne présente aucun intérêt et un coût trop important. La population vers laquelle les études se sont concentrées est celle des femmes à risque élevé de cancer du sein (1). Cette notion de risque à été précisée par des études épidémiologiques et l’intérêt de l’IRM étudié dans 6 études prospectives, non randomisées. Étude canadienne (3) • Démarrée en 2001. • 236 patientes volontaires, âgées de 25 à 65 ans, testées positives pour BRCA, sélectionnées par consultation génétique. • Durée de l’étude : 3 ans. • Procédure annuelle : mammographie, échographie et IRM mammaire. • 22 cancers détectés dont 50 % de taille < 1 cm et 13 % d’envahissement ganglionnaire. Étude italienne (4) • Démarrée en 2002. • 105 patientes volontaires, sélectionnées par consultation génétique, dont 27 % testées positives pour BRCA. • Durée de l’étude : 2 ans. • Procédure annuelle : mammographie, échographie et IRM mammaire. • 8 cancers détectés dont 50 % de taille < 1 cm et 13 % d’envahissement ganglionnaire. Étude hollandaise (5) • Début en 2003. • 1 909 femmes, âgées de 25 à 70 ans, sélectionnées par consultation génétique, présentant toutes un risque relatif > 15 %, dont 19 % testées BRCA+. • Procédure annuelle : examen clinique, mammographie, échographie et IRM mammaire. • Durée de l’étude : 3 ans. • 50 cancers sont découverts, dont 43 % sont de taille < 1 cm et 33 % présentent un envahissement ganglionnaire. • La mammographie est supérieure à l’IRM dans cette étude pour le CCIS. Étude allemande (6) • Durée de l’étude : 5 ans (1996-2001). • Étude prospective concernant 529 patientes volontaires, présentant un risque relatif > 20 %, sélectionnées par consultation génétique. • Âge moyen : 38 ans. • Procédure annuelle : examen clinique, mammographie, échographie et IRM mammaire. • 43 cancers, dont 16 % N+, un cancer d’intervalle. • Les auteurs proposent de remplacer la mammographie par l’IRM dans le dépistage de cette population. Étude anglaise (7) • Durée de l’étude : 3 ans • Étude prospective concernant des patientes volontaires, présentant un risque relatif > 25 %, dont 19 % de femmes testées BRCA positives, sélectionnées par consultation génétique. • Procédure annuelle : examen clinique + mammographie + échographie + IRM mammaire. • 45 % des cancers découverts sont de taille < 1 cm, 14 % d’envahissement ganglionnaire, deux cancers d’intervalle. • Les auteurs proposent de remplacer la mammographie par l’IRM dans le dépistage de cette population. Autres études • Étude australienne (8). • Étude réalisée aux États-Unis (tableau 2) Efficacité du dépistage IRM dans ces études (tableau 2) Ces études montrent que la supériorité de l’IRM mammaire comparativement aux autres techniques est particulièrement élevée ; au-delà des biais méthodologiques de ces études (faibles effectifs, durée d’étude courte, protocoles variés, etc.), cette constatation semble liée à une baisse des performances de la mammographie dans cette population, composée de femmes jeunes, non ménopausées. • Sensibilité de l’IRM : 71 à 100 % – Contre 16 à 40 % pour la mammographie. – Contre 16 à 40 % pour l’échographie. – Sensibilité de l’IRM pour le CCIS : 71 à 77 %. • Faux positifs et taux de biopsie – La spécificité de l’IRM est inférieure à celle de la mammographie dans toutes les études. – Taux de rappel (ACR3) : 8 à 15 %. – Taux de biopsie (ACR4) : 3 à 15 %. – Valeur prédictive des biopsies : 20 à 40 %. Compliance et adhésion Une étude parallèle, s’intéressant à l’impact psychologique de ce dépistage annuel, a été menée sur 611 femmes de l’étude anglaise (7) : 89 % des femmes surveillées souhaitent poursuivre contre 1 % des femmes qui souhaitent arrêter. Il n’y a pas d’effet sur l’anxiété globale, qui est de toute façon importante. Cet aspect n’est pas négligeable, car l’introduction de l’IRM dans la surveillance systématique, du fait de sa faible spécificité, est responsable d’un taux de faux positifs important. Ces faux positifs engendrent un certain nombre de bilans complémentaires (reprise du bilan conventionnel de manière ciblée, biopsies percutanées guidées, procédures chirurgicales, etc.). Prérequis du dépistage par IRM La mise en place d’un dépistage adapté à des populations dont le risque de pathologie mammaire est élevé, nécessite un certain nombre de conditions : – des radiologues formés et entraînés à l’interprétation de l’IRM mammaire et capables d’effectuer un bilan de deuxième intention (mammographie et échographie ciblées en vue) ; – la possibilité d’effectuer en routine des macrobiopsies et des repérages préopératoires sous IRM. Ces techniques de prélèvement et de repérage préopératoire souffrent, actuellement, d’un manque de diffusion. Réalisées dans peu de centres en France, essentiellement en raison du temps nécessaire pour exécuter ces gestes et de la faible disponibilité de l’IRM dans notre pays, l’organisation en réseau semble la seule alternative, cette activité spécifique étant confiée aux centres référents ayant acquis faisabilité et expérience. Population éligible au dépistage des cancers du sein par IRM annuelle (en plus de la mammographie annuelle) En 2007, l’American Cancer Society a publié des recommandations pour le dépistage par IRM en complément de la mammographie chez les femmes à risque élevé(9). Dépistage annuel par IRM recommandé en complément de la mammographie • Mutation BRCA identifiée. • Femme apparentée au premier degré d’un BRCA, mais non évaluée personnellement. • Risque de cancer du sein cumulé sur la vie ≥ 20-25 % (établi d’après les divers scores disponibles, lors d’une consultation génétique). • Syndrome de Li-Fraumeni et femmes apparentées au premier degré (mutation TP53). • Syndromes de Cowden et Bannayan-Riley-Ruvalcaba et femmes apparentées au premier degré (mutation PTEN). • Irradiation thoracique (Hodgkin) entre 10 et 30 ans, pour des traitements antérieurs aux techniques d’irradiation actuelles. Pas d’argument suffisant pour recommander le dépistage annuel par IRM • Risque de cancer du sein cumulé sur la vie compris entre 15 et 20 %. • Carcinome lobulaire in situ (RR > 20 %) et hyperplasie lobulaire atypique. • Hyperplasie canalaire atypique. • Seins hétérogènes ou très denses à la mammographie. • Femme avec une histoire personnelle de cancer du sein (dont le CCIS) : RR environ 1 % par an. Dépistage IRM non recommandé • Femme avec un risque de cancer du sein cumulé sur la vie < 15 %.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :