Publié le 06 fév 2013Lecture 7 min
Syndrome des ovaires polykystiques : intérêt et limite des explorations
H. BRY-GAUILLARD, Médecine de la Reproduction, CHIC Créteil Endocrinologie et Reproduction, CHU Bicêtre
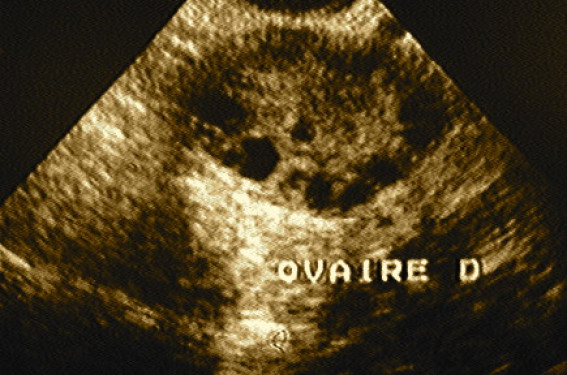
Le SOPK est une endocrinopathie fréquente : 5 à 10 % des femmes seraient atteintes. Elle représente la première cause d’hirsutisme et une cause majeure d’anovulation. Le SOPK est un syndrome hétérogène. C’est pourquoi sa définition, toujours utilisée actuellement, est pragmatique et issue du consensus de Rotterdam de 2003. Les critères actuellement utilisés font l’objet d’une réévaluation, notamment le critère échographique du nombre de follicules antraux, actuellement obsolète(1).
Le SOPK présente 3 composantes principales impliquées dans la physiopathologie du syndrome : l’hyperandrogénie, l’altération de la folliculogenèse et les anomalies métaboliques fréquemment associées mais non incluses dans la définition du syndrome (figure 1)(2). Les dosages hormonaux permettent l’évaluation de l’hyperandrogénie, ont un intérêt dans la démarche diagnostique et participent, avec l’échographie pelvienne, à l’évaluation du trouble de l’ovulation. Ils sont parfois difficiles à interpréter, par exemple lorsque le SOPK est masqué par une aménorrhée hypothalamique comme nous le montrons à la fin de cet article. Figure 1. Hypothèses physiopathologiques du SOPK. Évaluation de l’hyperandrogénie Le SOPK représente une cause majeure d’hirsutisme (figure 2)(3). Pour certaines sociétés savantes notamment américaines, l’hyperandrogénie reste un critère essentiel au diagnostic de SOPK. Pourtant, dans la métaanalyse de ce groupe incluant 5 659 patientes présentant une oligoaménorrhée et un aspect échographique de SOPK, on note que seules 37 % avaient une testostérone totale augmentée(4). Ce critère reste donc controversé. Cependant, l’évaluation de l’hyperandrogénie est utile, notamment dans la recherche de diagnostic différentiel du SOPK. La figure 3 représente la démarche diagnostique devant une hyperandrogénie clinique selon le dosage de testostérone totale(5). Le dosage de testostérone est recommandé en première intention, car : – il est le principal androgène actif circulant, – il est corrélé à l’importance de l’hirsutisme, – il est essentiel au diagnostic de tumeur androgénosécrétante. Figure 2. SOPK, une cause majeure d’hirsutisme. La méthode actuellement recommandée et utilisée en routine est le dosage radio-immunologique (avec, si possible, une extraction préalable), la méthode de référence, la spectométrie de masse, restant lourde et coûteuse. Les limites de ce dosage sont le manque de précision et une variabilité des résultats des trousses utilisées à ces niveaux bas de concentration de testostérone(5). Le dosage d’androstènedione est le plus souvent augmenté du fait d’une biosynthèse accrue de l’androstènedione par les cellules de la thèque. Le rapport androstènedione/ testostérone est quasi constamment > 1. Le dosage de 17 OH-progestérone (17 OHP) en début de phase folliculaire doit être réalisé afin d’écarter un bloc en 21 hydroxylase. Un taux de 17 OHP > 2 ng/ml de base et > 10 ng/ml après Synacthène® évoque le diagnostic de bloc en 21 hydroxylase et impose un séquençage du gène CYP21(6). Un hypercorticisme doit être recherché selon la clinique. Dans un contexte d’hirsutisme récent et/ou d’hyperandrogénie majeure, un dosage de SDHEA élevé orientera vers une étiologie surrénalienne (figure 3). Figure 3. Arbre décisionnel devant une hyperandrogénie clinique en fonction du taux de testostérone totale. Dosages des gonadotrophines associées à l’estradiol Dans le cadre de l’oligo-anovulation, les dosages réalisés en début de cycle (spontané ou induit par progestatif) permettent d’éliminer un hypogonadisme hypogonadotrope et une insuffisance ovarienne (tableau). Le dosage de prolactine (PRL) élimine une hyperprolactinémie. Dans le SOPK, la PRL peut être légèrement augmentée. Classiquement, la LH est modérément élevée dans environ la moitié des cas avec un rapport LH/FSH > 1, mais ceci ne constitue pas un critère diagnostique. Le test à la GnRH est inutile : il montre typiquement une réponse explosive de la LH après stimulation par GnRH. Dosages de l’AMH et compte de follicules antraux à l’échographie Le seuil du nombre de follicules antraux proposé en 2003 lors de la conférence de consensus sur la définition du SOPK est remis en question du fait des avancées technologiques importantes de l’échographie ces 10 dernières années. L’échographie pelvienne endovaginale avec les équipements actuels permet de visualiser et de comptabiliser (notamment en 3 D) les petits follicules antraux (CFA) de façon plus précise. L’équipe du Pr Dewailly a proposé comme seuil un compte de follicules antraux de 19/ovaire, permettant, dans son étude récente, une bonne performance diagnostique (240 patientes évaluées ; sensibilité 81 %, spécificité 92 %)(1). L’AMH est un peptide secrété par les cellules de la granulosa des follicules primo-secondaires et des petits follicules antraux. Sa sécrétion est maximale dans les follicules mesurant 1 à 4 mm dans l’espèce humaine. Elle pourrait jouer un rôle dans l’arrêt du développement folliculaire dans le SOPK. Le taux plasmatique d’AMH est nettement augmenté dans le SOPK du fait de l’augmentation du nombre de follicules, mais également d’une sécrétion plus importante au sein de chacun de ces follicules(7). La concentration plasmatique d’AMH semble être un reflet de la sévérité du SOPK(7). Le taux d’AMH est étroitement corrélé au CFA et un seuil de 5 ng/ml (35 pmol/l) a été retenu par l’équipe du Pr Dewailly comme étant optimal, avec une sensibilité de 92 % et spécificité de 97 %(1). Le dosage d’AMH pourrait être inclus à l’avenir dans la définition du SOPK, au même titre que le CFA. Ces seuils d’AMH et de CFA doivent cependant être validés par d’autres études. Cas de diagnostic parfois difficile Certaines situations peuvent rendre le diagnostic de SOPK difficile. C’est le cas lorsque le SOPK est masqué par une aménorrhée hypothalamique : le déficit gonadotrope induit par un sous-poids ou une balance énergétique défavorable, est responsable de taux d’androgènes et de gonadotrophines faussement normaux, voire bas. Le tableau complet de SOPK peut alors être démasqué lors d’une modification de l’hygiène de vie (diminution du sport ou reprise de poids) ou lors d’une induction de l’ovulation (figure 4)(8). Parmi les patientes présentant un tableau d’aménorrhée hypothalamique (AH), les paramètres tels que l’IMC, la LH, la testostérone seraient significativement plus élevés dans le groupe AH + SOPK(9). Le taux d’AMH pourrait, là encore, aider dans le dépistage du SOPK sous-jacent, car il est relativement indépendant du contrôle gonadotrope. Le dépistage du terrain SOPK dans l’AH a un grand intérêt, car il permet d’être particulièrement vigilant lors du traitement d’induction de l’ovulation du fait de risque important de développement multifolliculaire (donc risque d’hyperstimulation et de grossesses multiples). À l’inverse, l’hyperthécose qui représente une forme sévère de SOPK par hyperplasie majeure du stroma et de la thèque, peut entraîner des taux d’androgènes élevés proches des taux tumoraux. La réalisation d’un cathétérisme ovarien est parfois nécessaire lorsque l’imagerie est négative pour affirmer le caractère bilatéral de la sécrétion en opposition à la sécrétion unilatérale dans le cas d’une tumeur ovarienne androgénosécrétante. Figure 4. Profil particulier - hypogonadisme avec dystrophie ovarienne sous-jacente(8).
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :





