Publié le 12 déc 2017Lecture 7 min
Comment rechercher un syndrome de Lynch ?
Anne-Sophie BATS, Chirurgie cancérologique gynécologique et du sein, Hôpital européen Georges-Pompidou, Paris
Le syndrome de Lynch doit être recherché chez toute patiente présentant un cancer de l’endomètre avant l’âge de 50 ans ou quel que soit l’âge chez une patiente dont un apparenté au premier degré a été atteint d’un cancer colorectal ou du « spectre HnPCC ».
Le syndrome de Lynch, anciennement appelé HNPCC (Human Non Polyposis Colorectal Cancer) est une prédisposition héréditaire aux cancers colorectaux (CCR). Le suivi des familles HNPCC a permis de mettre en évidence une association avec des tumeurs d’autres localisations. Il prédispose donc, pour ce qui est de la femme, également au cancer de l’endomètre et au cancer de l’ovaire et dans l’ensemble de la population à risque au cancer de l’estomac, de l’intestin grêle, des voies excrétrices urinaires, des voies biliaires, de la peau (syndrome de Muir-Torre, variante du syndrome de Lynch avec atteintes cutanées), ainsi que du cerveau.
Définition clinique du syndrome de Lynch
Le syndrome de Lynch est défini cliniquement par les critères d’Amsterdam, qui ont été initialement définis pour poser le diagnostic de syndrome de Lynch dans des familles à risque de cancer colorectal (CCR). Ils ont ensuite évolué (critères d’Amsterdam II) pour intégrer les autres risques tumoraux. Leur définition répond à la présence d’au moins trois apparentés avec un cancer du spectre restreint :
– l’un est apparenté au premier degré avec les deux autres ;
– au moins deux générations atteintes ;
– au moins un cancer diagnostiqué avant l’âge de 50 ans ;
– une polypose adénomateuse familiale est exclue ;
– la tumeur doit être vérifiée.
Génétique du syndrome de Lynch
Le syndrome de Lynch correspond à une mutation germinale des gènes du système MMR (MisMatch Repair) impliqué dans la réparation de mésappariements de l’ADN. Les gènes actuellement connus sont les gènes MLH1, MSH2, MSH6 et PMS2. La mutation de l’un de ces gènes entraîne un phénotype tumoral particulier avec un défaut d’expression des protéines correspondantes, mise en évidence par immunohistochimie, ainsi qu’une instabilité tumorale retrouvée au niveau des séquences micro-satellitaires de l’ADN (MSI-H pour MSI-high).
L’étude somatique est une étapeclé dans la stratégie diagnostique. En présence d’une tumeur de phénotype stable sans perte d’expression protéique, le diagnostic de syndrome de Lynch peut être exclu. En revanche, en cas de tumeur instable avec perte d’expression de l’une des protéines MMR, il existe une indication de recherche de mutation au niveau sanguin.
Quand recherche le syndrome de Lynch ?
Concernant les tumeurs colorectales, les critères de Besthesda ont été définis pour la recherche d’instabilité sur la tumeur. Ils répondent aux critères suivants :
– CC < 50 ans ;
– second CCR synchrone ou métachrone ;
– second cancer du spectre HNPCC élargi ;
– anatomopathologie évocatrice et MSI < 60 ans ;
– CCR avec au moins 1 parent au 1er degré présentant une tumeur du spectre HNPCC < 50 ans ;
– CCR avec au moins 2 parents au 1er ou 2e degré présentant une tumeur du spectre HNPCC, indépendamment de l’âge. Concernant les tumeurs de l’endomètre, il existe une indication de recherche d’instabilité des microsatellites au niveau tumoral pour toute patiente présentant un cancer de l’endomètre avant l’âge de 50 ans, ou quel que soit l’âge, ou quel que soit l’âge chez une patiente dont un apparenté au premier degré a été atteint d’un cancer colorectal ou du « spectre HNPCC ».
Risque de cancers gynécologiques
L’étude de cohorte française ERISCAM, portant sur les familles avec mutation du gène MMR, a retrouvé un risque cumulé à l’âge de 70 ans de cancer de l’endomètre de 33 %, de cancer colorectal de 31 % et de cancer de l’ovaire de 9 %. Il est intéressant de noter que ces pourcentages varient en fonction de la mutation retrouvée. Ainsi, la mutation MLH1 est celle associée au plus grand risque cumulé à l’âge de 70 ans de cancer de l’endomètre (54 %), suivie de la mutation MLH2 (21 %) et MSH6 (16 %). Concernant les cancers colorectaux, le risque est le plus important avec la mutation MSH2 (48 %). En ce qui concerne le cancer de l’ovaire, il existe un risque cumulé à l’âge de 70 ans de 20 % en cas de mutation MLH1 et de 24 % en cas de mutation MSH2. En cas de mutation MLH6, le risque est de 1 %. Dans cette étude, l’âge médian de survenue des cancers de l’endomètre était de 49 ans et des cancers de l’ovaire de 44 ans. Il faut noter par ailleurs qu’aucun cas de cancer gynécologique n’est survenu avant l’âge de 40 ans.
Caractéristiques clinico-pathologiques des cancers gynécologues
Les caractéristiques clinicopathologiques des cancers de l’endomètre, quoique peu étudiées, retrouvent un âge de survenue jeune. Ce cancer est souvent sentinelle, c’est-à-dire qu’il s’agit du premier cancer survenant en cas de syndrome de Lynch. Il peut être synchrone d’une autre tumeur ou métachrone (plusieurs tumeurs successivement chez une même patiente). La majorité des tumeurs sont de type I, endométrioïde, mais il existe relativement plus de cancers de type II non endométrioïdes que dans la population générale. Il existe également davantage de stades II et la localisation de la tumeur au niveau de l’isthme utérin est assez évocatrice et est retrouvée dans 10 à 15 % des cas. Concernant les caractéristiques clinico-pathologiques des cancers de l’ovaire, cette tumeur survient également à un âge jeune. Il s’agit également de tumeurs synchrones ou métachrones. Le type histologique est essentiellement un adénocarcinome endométrioïde, à cellules claires, ou peu différencié. La majorité des tumeurs sont découvertes à un stade précoce et sont habituellement de bon pronostic.
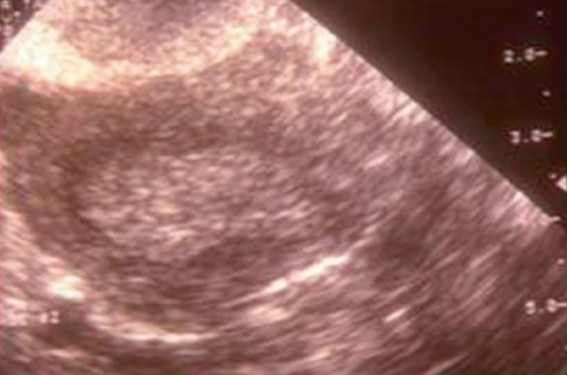
Figure 1. Échographie pelvienne.
Dépistage gynécologique
En raison du risque élevé de développer un cancer et de l’âge jeune de survenue, le dépistage gynécologique apparaît intéressant, quoique l’analyse de la littérature n’ait pas permis de prouver son bénéfice. Les outils de dépistage utilisés sont l’échographie pelvienne, la biopsie d’endomètre et l’hystéroscopie diagnostique.
• L’échographie pelvienne présente des limites dans la mesure où elle est opérateur dépendante et également en raison de la variation de l’épaisseur de l’endomètre en fonction du cycle menstruel.
• La biopsie d’endomètre est un examen qui apparaît très pertinent avec néanmoins comme limites d’être potentiellement mal toléré, ainsi qu’ininterprétable pour certains prélèvements.
• Enfin, concernant l’hystéroscopie diagnostique, très peu d’équipes ont évalué cet examen en raison principalement de la mauvaise tolérance supposée des patientes. Il apparaît néanmoins dans les études publiées que celle-ci est associée à une excellence sensibilité.
Les recommandations de surveillance gynécologique actuelles européennes sont de débuter le suivi à l’âge de 35 ans, annuellement, avec réalisation d’une échographie pelvienne et d’une biopsie d’endomètre. L’hystéroscopie est en option. Ces recommandations soulignent néanmoins le faible niveau de preuve des études. Dans tous les cas, il convient d’informer les patientes de la nécessité de consulter sans délai en cas de ménométrorragies, puisque la quasi-totalité des lésions précancéreuses et des cancers sont symptomatiques. En cas de dysplasie avérée mise en évidence, une hystérectomie doit être réalisée.
Chirurgie prophylactique
En dehors du dépistage gynécologique, la chirurgie prophylactique peut également être proposée aux patientes ayant accompli leur projet parental. Celle-ci est réalisée après un délai de réflexion, la proposition de consultation avec une psychologue et la réalisation d’un bilan opératoire. Elle consiste en une hystérectomie avec annexectomie bilatérale, idéalement réalisée par voie cœlio-vaginale. Il faut informer les patientes des En dehors du dépistage gynécologique, la chirurgie prophylactique peut également être proposée aux patientes ayant accompli leur projet parental. Celle-ci est réalisée après un délai de réflexion, la proposition de consultation avec une psychologue et la réalisation d’un bilan opératoire. Elle consiste en une hystérectomie avec annexectomie bilatérale, idéalement réalisée par voie coelio-vaginale. Il faut informer les patientes des conséquences de l’intervention qui entraîne l’impossibilité de toute grossesse ultérieure ainsi que la ménopause précoce. Il est néanmoins possible de proposer un traitement hormonal substitutif.
En conclusion
Le syndrome de Lynch est non seulement une prédisposition au cancer colorectal, mais également, pour ce qui concerne la gynécologie, au cancer de l’endomètre et de l’ovaire. Celui-ci peut concerner les femmes jeunes en âge de procréer, ce qui peut poser la question d’un traitement conservateur. Le dépistage gynécologique, quoique non validé, est recommandé. Tout saignement anormal nécessite une consultation en urgence. La chirurgie prophylactique demeure la meilleure option pour éliminer tout risque de survenue de cancer de l’endomètre.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :





