Publié le 04 fév 2021Lecture 8 min
Quand les lymphocytes NK (natural killer) de la décidua pratiquent l’injection intracytoplasmique (de granulysine)
D. ROTTEN, Paris
Au cours de la gestation, le système immunitaire maternel doit répondre à deux impératifs contradictoires : maintenir la capacité d’attaquer les agresseurs microbiens, bactéries, virus, champignons et parasites ; et en même temps, s’adapter à la présence d’antigènes étrangers que l’organisme maternel doit « tolérer », à savoir les antigènes issus des gènes paternels. Mais la tolérance a un prix : elle facilite les agressions microbiennes.
D’où la question : de quelle manière les cellules immunocompétentes maternelles arrivent-elles à conserver une activité cytotoxique, leur permettant d’être actives contre les différents agresseurs, sans que les cellules hôtes soient tuées ? Des progrès récents concernant le mode de fonctionnement des lymphocytes NK ont mis en évidence un mécanisme d’action original au niveau de la décidua.
Quelques protagonistes
Une délicate parie d’équilibre se joue donc au niveau de l’interface materno-fœtale, cellules déciduales maternelles d’une part, et cellules trophoblastiques — d’origine fœtale —, d’autre part.
Cellules trophoblastiques
Le placenta se forme quand des cellules dérivées du cytotrophoblaste fusionnent pour former des cellules plurinucléées, constituant le syncytiotrophoblaste. Celui-ci forme une couche continue qui borde les villosités libres. C’est à ce niveau que se produisent les échanges gazeux et métaboliques entre mère et fœtus. Les cellules de cytotrophoblaste persistent, sous forme d’une couche qui, avec l’avancement de la gestation, devient discontinue au niveau des villosités libres (figure 1).
Les cellules de cytotrophoblaste constituent également les villosités crampon, qui ancrent le tissu fœtal à l’utérus. Enfin, il existe des cellules trophoblastiques extra-villeuses. Elles pénètrent le tissu décidual. Ce sont elles qui sont à l’origine du remodelage des artères spiralées, permettant l’augmentation de leur débit sanguin, nécessaire au bon déroulement de la gestation.
Lymphocytes cytotoxiques
Des lymphocytes cytotoxiques sont présents en grand nombre dans la décidua. Au premier trimestre, ce sont les lymphocytes NK (natural killer) qui sont particulièrement nombreux. Au fur et à mesure que se déroule la gestation, les lymphocytes T cytotoxiques CD8+ deviennent prépondérants. Quand un lymphocyte cytotoxique reconnaît une cellule infectée, deux mécanismes se déclenchent : la libération de cytokines et une action cytotoxique directe.
Les lymphocytes T cytotoxiques CD8+ font partie de l’immunité adaptative (ou spécifique). Leur activation nécessite 3 à 5 jours. Ils détruisent par cytolyse les cellules étrangères ou exprimant un antigène étranger au « soi ». La reconnaissance de ces antigènes étrangers nécessite leur association à un antigène du complexe majeur d’histocompatibilité, HLA-A et HLA-B. L’embryon présente à la surface de ses cellules des protéines HLA différentes de celles de sa mère, puisque la moitié de ses gènes sont d’origine paternelle. Il devrait donc être attaqué et éliminé. Mais les cellules trophoblastiques n’expriment pas à leur surface les antigènes du complexe majeur d’histocompatibilité classique. En revanche, elles expriment des antigènes d’histocompatibilité de type HLA-C et des antigènes d’histocompatibilité non classiques comme HLA-E et HLA-G. C’est en particulier le cas des cellules du trophoblaste extra-villeux. L’expression de HLA-G est essentielle. Il s’agit d’un antigène monomorphe. Il exerce une fonction immunosuppressive. Ainsi, les lymphocytes T n’identifient pas les cellules trophoblastiques comme étrangères, et elles échappent à leur action cytotoxique.
Les cellules NK sont des lymphocytes non-B, non-T. Elles sont un maillon essentiel de l’équilibre immunitaire fœto-maternel. On reconnaît deux populations : les cellules NK périphériques ou NKp (sang, rate…) et les cellules NK déciduales ou NKd. En effet, de nombreuses cellules NK envahissent le côté maternel du placenta (la décidua), où elles sont très abondantes, en particulier au premier trimestre de la grossesse.
Bien que faisant partie de la famille des lymphocytes, les cellules NK relèvent de l’immunité innée, encore appelée naturelle (d’où leur dénomination de « natural killer »). Elles agissent immédiatement, sans nécessiter de première présentation d’antigènes. Au niveau de la décidua, leur action cytotoxique s’exerce sur les cellules dépourvues de marqueurs HLA classique. Les cellules NKd sont dotées d’un système de reconnaissance du marqueur HLA-G, qui inhibe leur action cytolytique vis-à-vis des cellules trophoblastiques normales.
Les cellules infectées présentent plusieurs caractéristiques communes, comme des perturbations de l’expression de protéines du complexe majeur d’histocompatibilité ou des signes moléculaires de stress cellulaire. Infectées, les cellules de trophoblaste deviennent « visibles » par les cellules immunes cytotoxiques.
Mécanisme d’action des cellules immunes tueuses
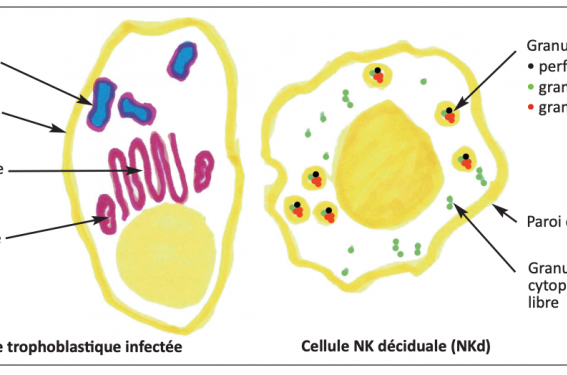
Les cellules tueuses sont riches en enzymes cytolytiques. Ces dernières sont principalement contenues dans des granules intra-cytoplasmiques (figure 2).
Ces derniers contiennent plusieurs familles de protéines protéolytiques. La perforine s’attaque essentiellement aux parois cellulaires riches en cholestérol, ce qui est le cas des cellules de mammifères, donc des cellules trophoblastiques. La cytolyse des parois de la cellule-cible qu’elle provoque permet aux autres enzymes contenues dans les granules, granulysine et granzymes, d’y pénétrer. La granulysine s’attaque aux parois cellulaires pauvres en cholestérol, ce qui est le cas des parois microbiennes (bactéries, champignons, parasites). Elle permet aux granzymes de s’introduire dans les bactéries attaquées. Les granzymes sont des protéases à sérine. Leurs cibles à l’intérieur des bactéries sont multiples : destruction du réticulum endoplasmique et des mitochondries, clivage de nombreux substrats essentiels au métabolisme et aux voies de synthèse cellulaires, activation de la cascade caspase, génération de radicaux superoxydes, interruption des voies de défense anti-oxydatives, etc.
Leur action aboutit à la mort cellulaire programmée des bactéries. Mais parallèlement, les granzymes vont induire la destruction de la cellule hôte par apoptose, en utilisant les mêmes mécanismes.
À noter, la granulysine est également présente dans le cytosol des cellules NKd.
Attaque classique (figure 3)
Quand un lymphocyte tueur, par exemple une cellule NKp, repère une cellule infectée ou transformée qu’il faut éliminer, il entre en contact avec elle grâce à des récepteurs d’adhésion cellulaire (intégrines), pour constituer une synapse immune.
Les granules cytotoxiques se dirigent vers la synapse immune. La perforine endommage la paroi de la cellule attaquée. Par exocytose, les granules cytotoxiques déversent leur contenu enzymatique, granulysine et granzymes, dans la cellule cible. La granulysine attaque la paroi cellulaire des bactéries présentes dans la cellule hôte et permet aux granzymes d’y pénétrer à leur tour. Les granzymes y déclenchent une microptose (processus de mort cellulaire programmée des bactéries), en provoquant des dommages essentiels à leur métabolisme. Parallèlement, les granzymes passées dans le cytoplasme de la cellule-cible attaquent les membranes des organelles intracytoplasmiques, comme les mitochondries et le réticulum endoplasmique, et les détruisent dans un processus de mort cellulaire programmée.
Ce mécanisme d’attaque directe permet donc la destruction des germes présents dans la cellule-cible. Mais les cellules hôtes sont également détruites.
Mécanisme des ponts cytoplasmiques (figure 4)
Au niveau placentaire, un mécanisme original de défense antimicrobienne vient d’être mis en évidence par Ângela C Crespo et coll. Plus discriminant, il permet la destruction de bactéries infectant les trophoblastes sans endommager les cellules hôtes. Pour arriver à cette constatation, les auteurs ont conduit une longue série d’expériences, présentées dans l’encadré.
Voici leur conclusion.
Quand une cellule NKd repère une cellule infectée, elle ne constitue pas avec elle une synapse immune classique. Il n’y a pas non plus d’activation des granules cytotoxiques et leur accumulation vers la zone de contact entre les deux cellules.
Par contre, on observe la création d’extensions cytoplasmiques, qui lient la cellule NKd à la cellule trophoblastique. Ces ponts intercellulaires sont de véritables nanotubes, dont le squelette est constitué d’acine. Ils permettent un transfert de la granulysine présente dans le cytoplasme des cellules NKd vers celui des cellules trophoblastiques (figure 4). Avec ce mécanisme, la seule enzyme transférée est donc la granulysine, qui attaque spécifiquement les parois bactériennes. Perforine et granzymes n’interviennent donc pas. Les germes sont attaqués sans que les cellules placentaires soient lésées.
Importance physiologique du phénomène
Ângela C Crespo et coll. ont donc mis en évidence l’existence, au niveau de l’interface fœto-maternelle, d’un mécanisme de lute anti-infectieuse compatible avec le maintien de la tolérance immunitaire placentaire. Ainsi, les lymphocytes NKd — présents dans la décidua — sont capables de transférer une enzyme lytique, la granulysine, vers l’intérieur de cellules trophoblasiques infectées par Listeria monocytogenes. Une fois dans le trophoblaste infecté, la granulysine cible les bactéries présentes et les détruit, en endommageant leur membrane. Le mécanisme en cause est un transfert direct, de cytoplasme à cytoplasme, par l’intermédiaire de ponts intercellulaires constitués par des nanotubes. L’opération ne nécessite pas de recours au phénomène habituel, l’activation des granules cytotoxiques présents dans les cellules cytolytiques, qui eux détruisent tout à la fois les bactéries et la cellule infectée.
Des expériences in vitro montrent que ce mode d’action est moins puissant que le mécanisme classique. Comme le transfert enzymatique par nanotubes, le mécanisme de cytotoxicité classique fait aussi intervenir la granulysine. Mais il met également en action les granzymes, famille d’enzymes qui détruisent les chaînes de transferts d’électrons, les voies de synthèse protéiques et les chaînes métaboliques essentielles des bactéries attaquées. On est donc en présence d’une limitation du pouvoir cytotoxique des principales cellules immunes cytotoxiques vis-à-vis des antigènes non maternels. Le développement de la tolérance immune au niveau de l’interface materno-fœtale, qui se traduit par l’absence de destruction des cellules placentaires infectées, a pour prix une limitation de la défense antibactérienne.
L’importance physiologique du phénomène n’est pas encore déterminée. Une piste est fournie par un modèle de souris transgénique. Spontanément, le patrimoine génétique des souris ne comporte pas le gène de la granulysine et elles n’expriment donc pas cette enzyme. L’infection expérimentale en début de gestation par Listeria monocytogenes chez des souris gestantes aboutit donc à l’avortement de la portée.
Lorsque la même expérience est répétée chez des souris génétiquement modifiées, chez lesquelles a été transféré le gène de la granulysine, la gestation se poursuit. Les mères mettent bas des souriceaux sains. Dans des conditions similaires, priver l’animal de perforine n’empêche pas la poursuite de la gestation.
Autre interrogation, comment le phénomène évolue-t-il au cours de la gestation ? Les cellules NKd sont les cellules immunes prépondérantes dans le placenta au premier trimestre de la gestation.
Au fur et à mesure que l’on s’approche du terme, les cellules NKd sont remplacées par des lymphocytes T CD8+. Or, ces cellules agissent selon un mécanisme d’action classique.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :





