Publié le 13 jan 2021Lecture 8 min
Sécheresse vaginale : estrogène, hydratant, lubrifiant ou laser ?
J. SALERNO, Nîmes
L’atrophie vulvo-vaginale (AVV) s’intègre dans le syndrome génito-urinaire de la ménopause (SGUM) associant des symptômes urinaires, vulvo-vaginaux et sexuels.
Certaines femmes pensent que souffrir de sécheresse vaginale est une fatalité faisant partie de l’avancée en âge. Pire encore, les patientes ménopausées brutalement suite à un traitement du cancer n’osent pas en parler. Pourtant, l’impact sur la qualité de vie et la sexualité peut être majeur.
En 2020, il est indispensable que l’information concernant l’AVV soit vulgarisée auprès des patientes, mais aussi des professionnels de santé. Les gynécologues doivent interroger les patientes à la recherche de symptômes d’AVV et savoir utiliser l’arsenal thérapeutique disponible.
Le traitement doit être d’autant plus précoce chez les patientes ménopausées brutalement suite à une chimiothérapie, une hormonothérapie, une ovariectomie ou une irradiation pelvienne.
L’AVV doit être traitée de manière globale en agissant sur la muqueuse vaginale, sa vascularisation, la sangle musculaire et l’écosystème vaginal. Le traitement de base associe au niveau vaginal de l’acide hyaluronique, des probiotiques et un traitement hormonal local. L’amélioration est progressive et un traitement d’entretien est souvent nécessaire, car le SGUM s’aggrave avec l’âge. En informer la patiente est indispensable à la bonne observance et l’efficacité de ces traitements locaux.
L’avènement du laser pourrait permettre de traiter différemment l’AVV, mais ce traitement n’est pas recommandé en première intention et doit être pratiqué dans le cadre d’essais cliniques.
Atrophie vulvo-vaginale
Physiopathologie
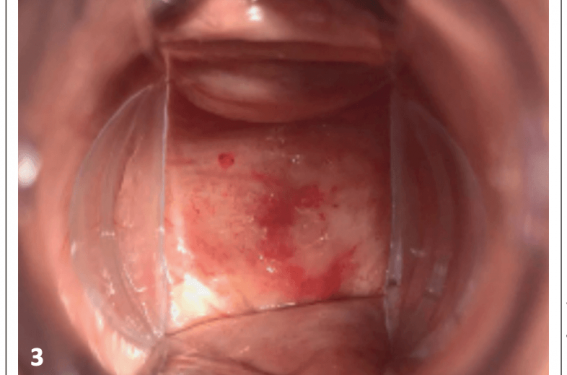
La baisse d’estrogène sérique est responsable d’une carence estrogénique et collagénique qui modifie la structure et l’épaisseur de l’épithélium vaginal avec à l’examen clinique une muqueuse pâle, lisse, fine et fragile (figures 1, 2 et 3).
Une réduction de l’introït vulvo-vaginal peut s’observer chez les femmes non ou peu sexuellement actives.
La diminution du taux de glycogène, en lien avec la faible épaisseur vaginale, et le défaut de colonisation vaginale des lactobacilles entraînent une baisse de production d’acide lactique et une augmentation du pH vaginal (> 5). Les femmes ménopausées sont donc plus à risque de vaginose bactérienne ou de pertes malodorantes.
L’hypoestrogénie diminue la vascularisation de l’épithélium vaginal et crée une baisse de l’hydratation par moindre transsudation.
Symptomatologie
La patiente se plaint d’une sensation de sécheresse avec prurit, irritation, inconfort, voire l’impression d’une brûlure vulvo-vaginale. Il existe une baisse de la lubrification pendant les rapports sexuels avec dyspareunie orificielle allant jusqu’à l’impossibilité d’avoir des rapports.
Dans certains cas, il ne semble pas exister de corrélation entre la gravité des symptômes de la patiente et la sévérité de l’atteinte clinique. Interroger la patiente à la recherche de symptômes d’AVV est donc primordial.
Examen clinique
Dans les AVV sévères (figures 1 et 2) l’examen au spéculum n’est pas indispensable lors de la première consultation. Il s’agit d’inspecter la vulve en déplissant la zone vulvovaginale délicatement afin d’inspecter le vestibule et les reliquats hyménéaux qui constituent les premières zones sensibles et symptomatiques. Cet examen vulvaire peut être suffisant pour entreprendre un traitement efficace sur l’AVV ; l’examen au spéculum sera réalisé lors d’une prochaine consultation. La compréhension de la plainte et de la douleur de la patiente permettra son adhésion au traitement local.
Nouveau concept thérapeutique
Les symptômes d’AVV sont réversibles avec un traitement local bien conduit. Toutefois en cas d’arrêt, l’AVV s’aggravant avec l’âge, les symptômes risquent de récidiver.
La prise en charge doit être globale. Elle comprend plusieurs étapes (tableau) et concerne la muqueuse vaginale, sa vascularisation, la sangle musculaire et l’écosystème vaginal.
Le traitement hormonal subsitutif ne soulage que 70 % des patientes ayant une AVV et n’est pas indiqué en cas d’AVV isolée (balance bénéfices/risques défavorable).
Traitement symptomatique
Hydratation de la muqueuse vaginale : topiques locaux
Les lubrifiants sont très riches en eau, silicone, huile minérale ou végétale et glycérine. L’hydratation ressentie est rapide, mais brève (le temps d’un rapport sexuel).
Les hydratants humidifient le vagin en mimant les sécrétions normalement présentes. Hydrophiles et insolubles, ils adhérèrent à l’épithélium vaginal et contribuent à retenir l’eau et à diminuer le pH. L’hydratation est rapide, de courte durée (moins de trois jours) et moins efficace que les estrogènes locaux.
L’acide hyaluronique améliore l’élasticité du tissu conjonctif et l’hydratation de la muqueuse. Il soulage rapidement les symptômes du SGUM avec une durée d’efficacité d’environ 3 jours(1).
Régulation du pH vaginal
Les probiotiques locaux ont pour objectif de restaurer le microbiote en diminuant le pH vaginal.
Ils permettent d’améliorer le confort vaginal et de réduire les vaginoses bactériennes. Seuls les lactobacilles ont démontré leur efficacité au niveau de l’écosystème vaginal. Il existerait une association synergique avec les estrogènes locaux sur le microbiote vaginal(2).
Traitement étiologique
Traitement hormonal local (THL)
Les estrogènes locaux ont démontré leur efficacité sur les symptômes du SGUM, quel que soit leur galénique (crème, ovule ou anneau vaginal)(3). Ils sont prescrits à la dose minimale efficace ; les patientes sont régulièrement suivies pour contrôler l’efficacité et la sécurité du traitement.
L’hydratation préalable de la muqueuse vaginale est indispensable avant d’introduire ces traitements sous peine d’une sensation de brûlure douloureuse chez les patientes ayant une AVV sévère, responsable le plus souvent d’un arrêt précoce du traitement.
L’hydratation est aussi primordiale, car plus l’épithélium vaginal est fin, plus le passage systémique des estrogènes augmente. En effet, on note à l’initiation du THL une augmentation du taux d’estradiol plasmatique suivie d’une diminution rapide. Pour autant, il n’a pas été démontré de surrisque de cancer du sein chez les patientes sous THL(4).
Chez les patientes ayant un antécédent de cancer du sein le THL est possible après étude de la balance bénéfices/risques et accord de l’oncologue, si la patiente accepte le traitement. Les études ne semblent pas montrer de surrisque de récidive du cancer du sein(5).
Prastérone vaginale
La prastérone est commercialisée en France depuis mai 2019. Il s’agit d’un précurseur de stéroïde, semblable à la déhydroépiandrostérone (DHEA) endogène humaine, converti au niveau vaginal en estrogène et androgène. Cet effet androgénique le différencie du THL et pourrait jouer un rôle dans la dysfonction sexuelle en augmentant le désir.
Rééducation pelvi-périnéale
Après restauration de la trophicité vaginale, elle permet de diminuer les symptômes urinaires du SGUM (urgenturie, incontinence), et d’améliorer la sexualité(6). La rééducation peut permettre également une éducation de la patiente, un apprentissage de la respiration profonde (traitement d’une éventuelle hypertonie des releveurs secondaire), et une augmentation de la vascularisation avec le travail musculaire et donc, indirectement, de l’hydratation vaginale.
Nouvelles technologies
En cas d’échec partiel ou total des traitements de première ligne ou si le THL est contre-indiqué, il faut pouvoir proposer à la patiente des traitements de deuxième intention.
Le laser vaginal (CO2 fractionné ou Erbium : YAG) consiste en une vaporisation de la couche superficielle de la muqueuse vaginale, entraînant une simulation des fibroblastes et de la néocollagenèse qui favorise la repousse d’une nouvelle muqueuse vaginale.
Les contre-indications sont une infection vulvo-vaginale en cours, un antécédent d’infection à papillomavirus ou un herpès génital et les troubles de la cicatrisation.
Les données de la littérature, bien que pauvres et de faible niveau de preuve, semblent montrer que le laser vaginal est aussi efficace que le THL sur les symptômes d’AVV en ayant un effet plus durable dans le temps(7). Cependant le manque de recul sur le laser et les risques rapportés dans certaines études (brûlure urétrale, cicatrice douloureuse) n’incitent pas à le recommander en première intention.
La photobiomodulation, technique indolore et présentant peu de contre-indications, paraît adaptée aux issus irradiés. La radiofréquence est aussi une alternative intéressante. Mais il n’existe que quelques séries observationnelles sur de faibles effectifs.
L’injection vestibulaire d’acide hyaluronique semble restaurer l’hydratation avec un effet durable.
Rien ne prouve à ce jour que les autres techniques injectables (plasma riche en plaquettes, graisse autologue) soient efficaces.
Toutes ces thérapies sont onéreuses et au banc d’essai. Le praticien doit être formé à l’utilisation de ces nouvelles technologies et les patientes prévenues des risques et des bénéfices de ces traitements qui ne sont actuellement pas recommandés en première intention par les sociétés savantes(8).
Conclusion
À l’heure actuelle, l’atrophie vulvo-vaginale ne doit plus être considérée comme une fatalité liée au vieillissement de la femme. Elle est, certes, physiologique, liée à l’âge et à la dégénérescence ovarienne, mais elle ne doit pas être négligée pour autant.
Les oncologues, les radiothérapeutes et les chirurgiens oncologues sont parfois en première ligne pour agir chez leurs patientes à risque d’AVV sévère, brutale et difficilement réversible ; ils doivent être sensibilisés et traiter leurs patientes avant l’apparition des premiers troubles. Les gynécologues, les sages-femmes et les médecins généralistes restent les inter locuteurs privilégiés des femmes et doivent dépister et traiter les patientes souffrant d’AVV.
La restauration d’une trophicité vulvo-vaginale passe par une trithérapie locale com posée d’acide hyaluronique, de lactobacilles et d’un traitement hormonal local. Ces traitements ont un coût non négligeable (seul le THL est remboursé), sont perçus comme contraignants (application quasi quotidienne de crème ou d’ovule et texture trop liquide des produits), et leurs effets sont aléatoires. L’indication du laser vaginal est à réserver en seconde intention, après échec de la trithérapie locale de première intention et en l’absence de contre-indications. Les patientes éligibles doivent être adressées à un praticien formé à la technique et participant à la recherche clinique.
Depuis janvier 2020 au CHU de Nîmes, nous menons une étude observationnelle prospective (OTTAPE) concernant les nouvelles technologies (laser vaginal, radiofréquence, photobiomodulation, injection d’acide hyaluronique)(9). Cet observatoire a pour objectif de colliger les données concernant les patientes traitées par ces nouvelles technologies afin d’en étudier les indications, l’efficacité et la survenue d’éventuels effets indésirables. Tout centre désireux d’y participer peut nous contacter.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :

